我們做科研的,大多數人都養過細胞,細胞樣本實驗周期短,成本低,我們在養細胞的時候不可避免的要用到培養基,比如微生物用到的 LB, M9 等,動物細胞用到的 DMEM 等,每種培養基的成分都不盡相同,那么你有沒有考慮過,培養基是如何給細胞提供營養的呢?那些 C 源 N 源到底是怎么維持細胞生長的呢?我們今天要分享的這篇文獻,就以谷氨酰胺為例,使用同位素追蹤的方法給大家展示在缺氧條件下,谷氨酰胺作為 C 源是如何維持腫瘤細胞生長的。
部分 介紹谷氨酰胺的重要性
當然了,先證明谷氨酰胺對細胞生長是很重要的,再來研究他的代謝,沒毛病。
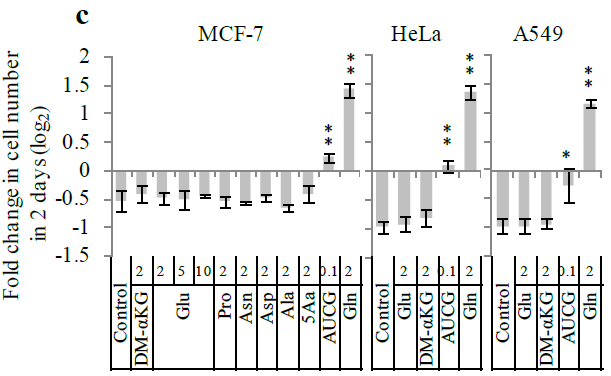
首先用添加了不同濃度、不同成分的培養基(Glu,AUCG,各種氨基酸)培養腫瘤細胞,發現培養基中若沒有谷氨酰胺,細胞死亡率會顯著上升,而添加了 AUCG 的培養基可以在谷氨酰胺缺失的情況下抑制細胞的死亡,說明谷氨酰胺與核苷的合成有關。由此,作者推論,谷氨酰胺是細胞生長所必須的物質。
那么在缺氧條件下細胞會將谷氨酰胺作為 C 源維持生長,但是谷氨酰胺也是生物體的 N 源,那么細胞會如何處理隨之而來的高濃度的 N 呢?
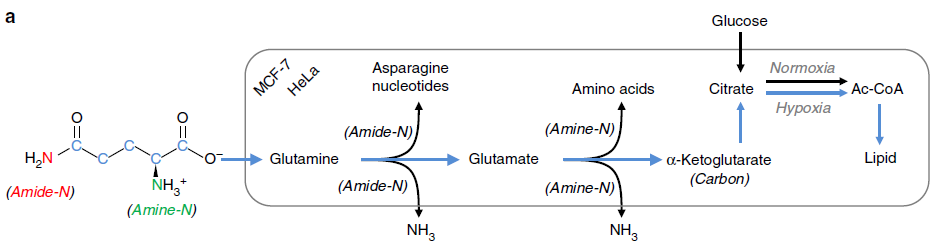
在缺氧條件下谷氨酰胺被用來做為主要的 C 源,尤其是脂質合成。
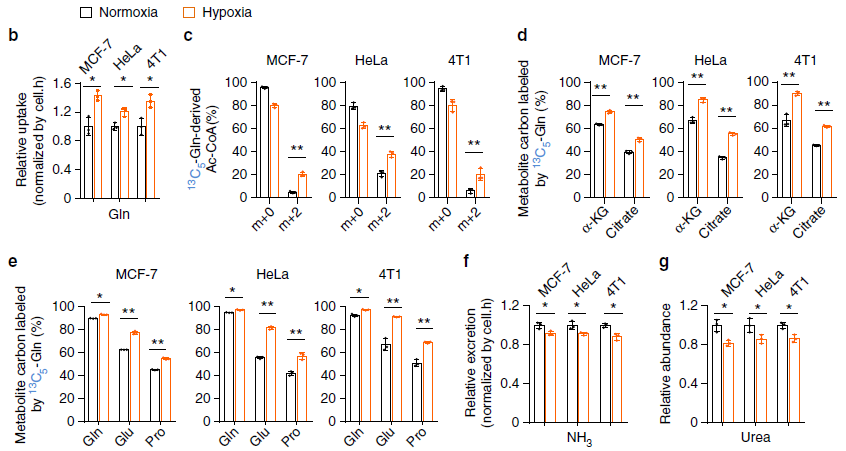
由上圖 b 可知缺氧條件下細胞對谷氨酰胺(Gln)吸收增加了。通過 13C-Gln 標記發現脂質前體 Ac-CoA 增加了(圖 c,m+0 減少,m+2 增加),其他下游物質如氨基酸等也增加了(圖 d,e)。這些數據表明缺氧時谷氨酰胺作為 C 源吸收增加了。接下來,作者試圖找到谷氨酰胺的 N 代謝。谷氨酰胺可以脫去氨基生成 NH3,但是對培養基的檢測發現 NH3 的量沒有升高反而下降了(圖 f),NH3 可以被代謝成尿素,但是培養基中尿素的含量卻下降了(圖 g),因此谷氨酰胺的 N 應該是被其他物質利用了。
第二部分 研究谷氨酰胺的代謝
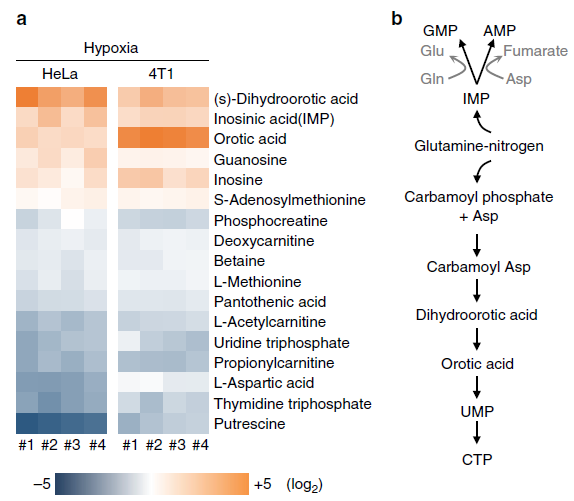
通過在缺氧條件下的含 N 代謝物的篩選,得到了 6 個顯著升高的物質,11 個顯著下降的物質。其中,五個顯著上調的物質:IMP、DOHA、OA、鳥嘌呤和肌苷參與了 nucleotide biosynthesis 通路,驗證結果也表明在 HeLa、MCF-7 和 4T1 細胞中 IMP(AMP 和 GMP 的前體)、carbamoyl-Asp、DHOA、OA 都顯著升高。這些結果表明缺氧導致細胞內核苷酸的前提累積,尤其是嘧啶前體,包括 carbamoyl-Asp、DHOA 和 OA。
?缺氧條件下谷氨酰胺的 N 富集在 DOHA 和 OA 上
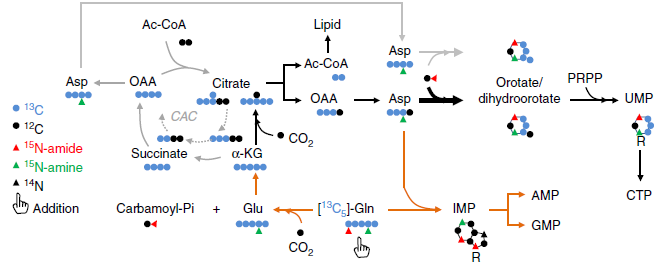
作者使用 N15 標記的谷氨酰胺來追蹤 N 的吸收。由上圖可知,酰胺基(Amine)上的 N 會轉移到 Asp、DOHA、OA、UMP、IMP 上,而氨基(Amide)上的 N 會轉移到 DHOA、OA、UMP、IMP 上。
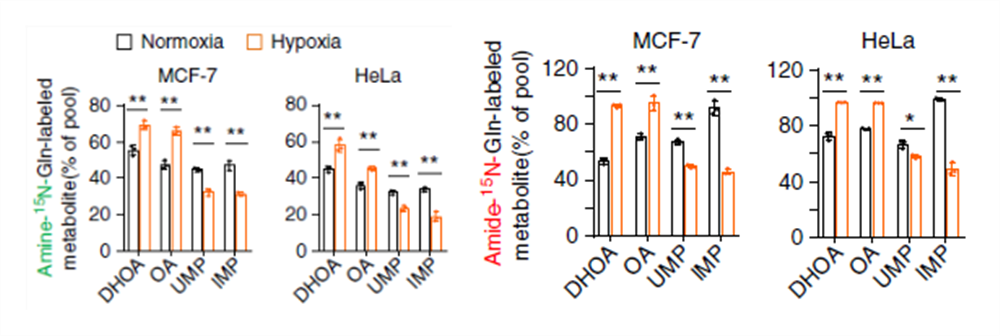
在缺氧條件下,標記的 DHOA 和 OA 含量顯著上升,說明谷氨酰胺的 N 富集于 DHOA 和 OA 上,但是 DHOA 和 OA 的代謝效率不高,因為下游產物 UMP 含量沒有增加。
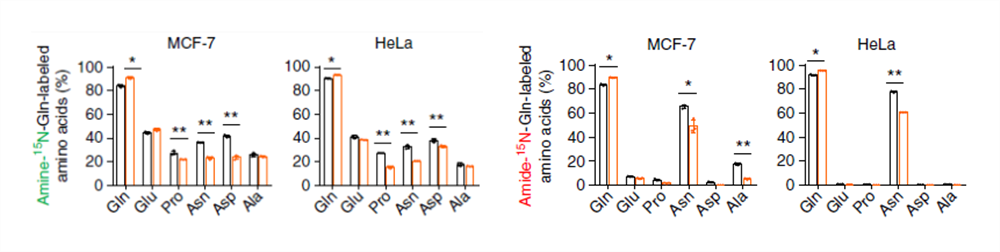
標記的 N 還可以在氨基酸中檢測到,但是在缺氧條件下,被標記的氨基酸含量都沒有升高,因此這些數據可以證明缺氧條件下谷氨酰胺的 N 富集于 DHOA 和 OA 上而不是氨基酸上。
?缺氧條件下促使天冬氨酸作為嘧啶前體
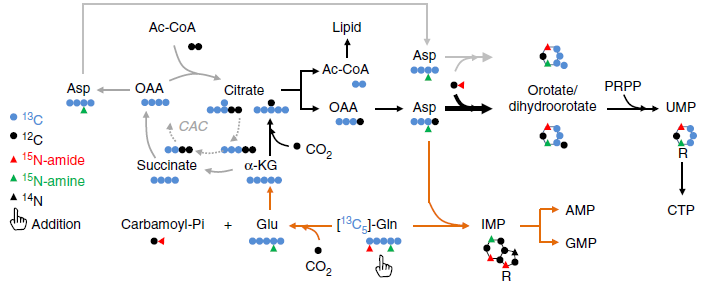
由上圖可知,谷氨酰胺的 C 在通過 TCA 循環和 α- 酮戊二酸羧化還原途徑轉移到天冬氨酸之后可以被合成為嘧啶。這兩條途徑可以通過檢測 C13-Gln 來源的乙酰輔酶 A,天冬氨酸,檸檬酸,DHOA 和 OA 來區分。正常條件下,谷氨酰胺的 C 進入 TCA 循環,可以生成 M+4 的 Asp,檸檬酸,DHOA 和 OA;在缺氧條件下,生成 m+2 的乙酰輔酶 A,m+3 的天冬氨酸,m+5 的檸檬酸,m+3 的 DHOA 和 OA 通過還原途徑生成;m+3 的 UMP 可以由兩條途徑都生成。
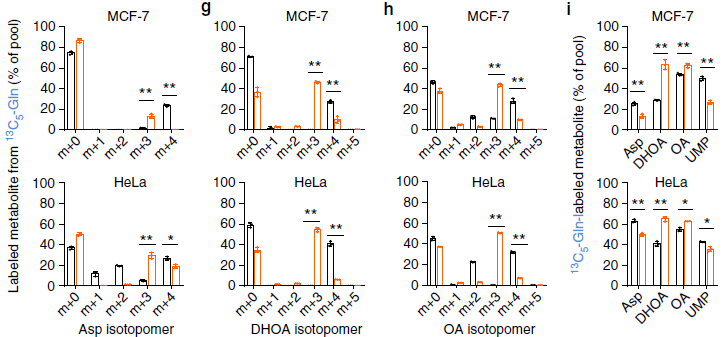
由上圖結果可知缺氧條件下谷氨酰胺的 C 通過還原途徑進入了乙酰輔酶 A、DHOA 和 OA,并且含量有所升高,因此缺氧條件促進了他們的合成。但 DHOA 的直接前體:天冬氨酸含量卻降低了,這可能與嘧啶合成通路中多個酶參與有關,為研究這個現象,作者使用 C13,15N-Asp 來追蹤天冬氨酸在嘧啶合成中的代謝。
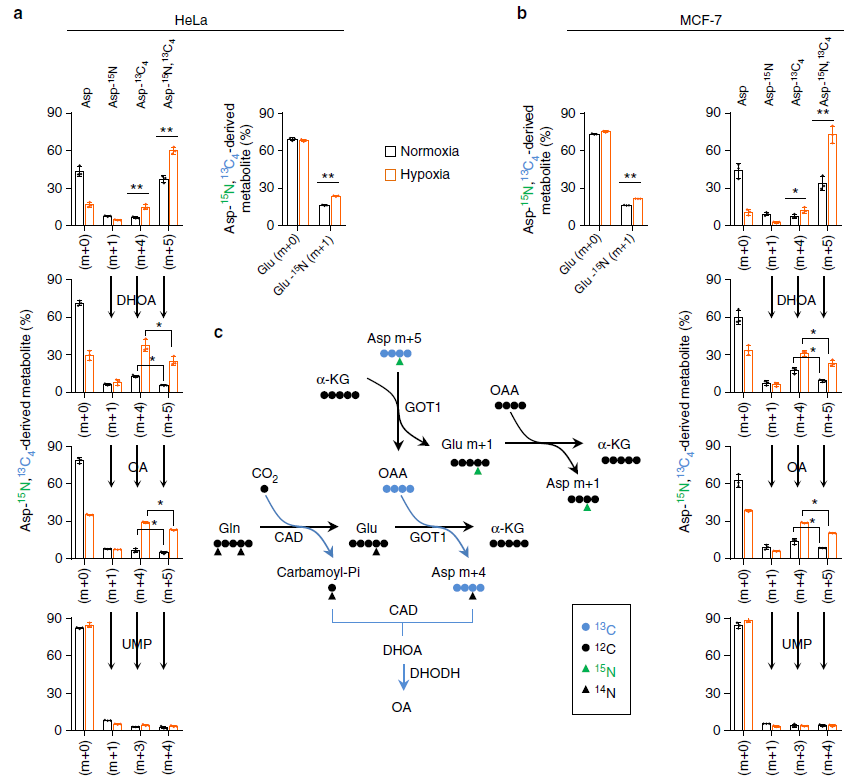
由上圖可知,檢測到了 m+5 的 Asp 表明細胞完全可以吸收外源的 13C-15N-Asp(圖 a),也檢測到了 15N-m+1 的谷氨酸和天冬氨酸,13C-m+4 的天冬氨酸(圖 a,b);缺氧使細胞吸收更多的天冬氨酸,有趣的是,正常條件下細胞并不能產生很多的 DHOA 和 OA, 但是在缺氧條件下 DHOA 和 OA 的含量都升高了(m+4,m+5 顯著升高),而且 m+4 的天冬氨酸生成 m+5 的 DHOA 和 OA 效率更高了,因此缺氧使天冬氨酸到 DHOA 和 OA 的途徑活性升高了,這也導致細胞內的天冬氨酸含量降低。
?DHOA 和 OA 是細胞生長必須的嗎?
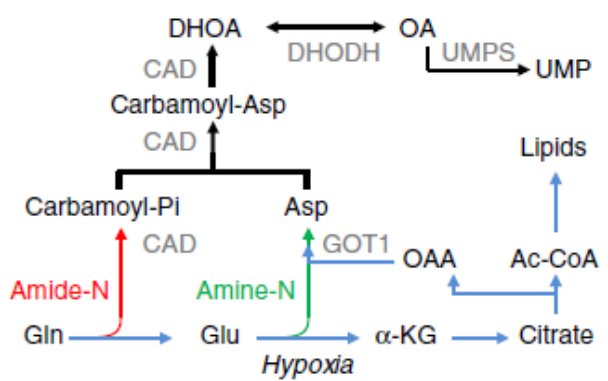
從上述結果來看,缺氧條件下大部分的谷氨酰胺都生成了 DHOA 和 OA,那么他們對細胞生存是必須的嗎?作者對 DHOA 和 OA 通路上的酶做了 knockdown,如 CAD、DHODH、GOT1。
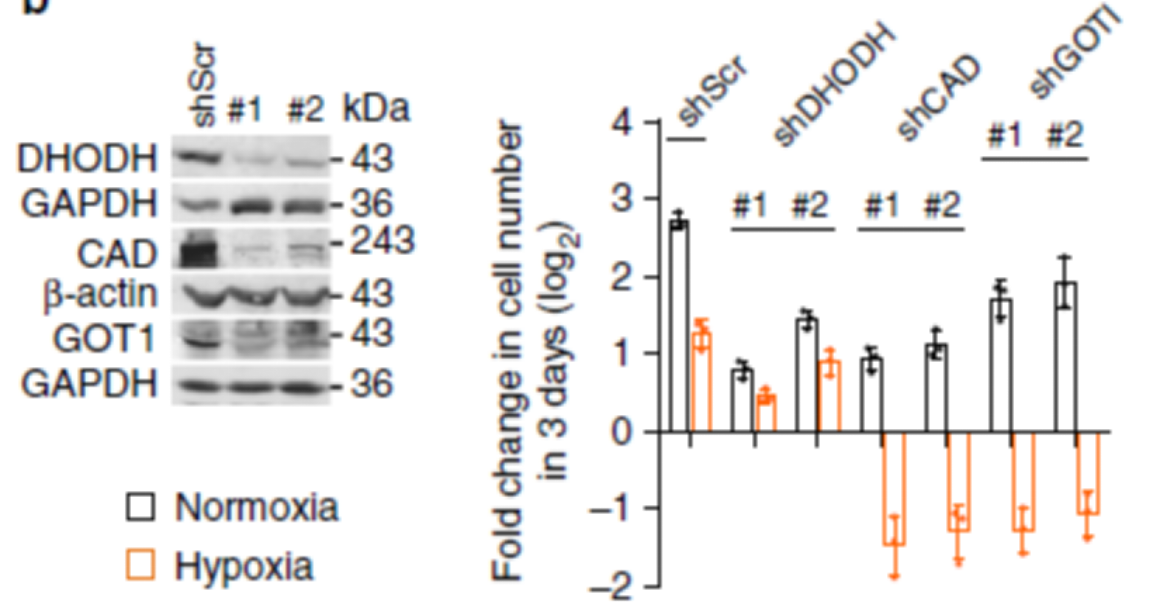
DHODH 和 CAD 是嘧啶合成的關鍵酶,因此他們的 knockdown 即使在正常條件下也明顯的影響了細胞的分化。相反的是,缺氧條件下,GOT1 的敲除輕微地影響了細胞的分化。而 CAD 和 GOT1 的敲除讓細胞無法生長,DHODH 的敲除只是稍微影響細胞的生長。這說明對于細胞來說,DHOA 才是不可缺少的,而不是 OA。
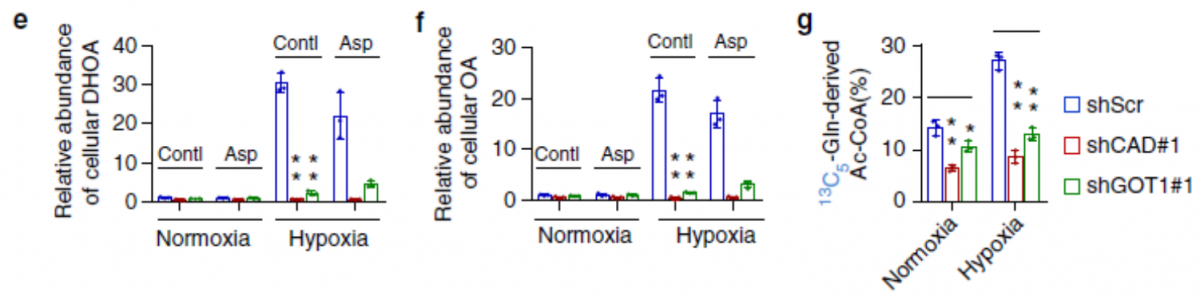
CAD 和 GOT1 的敲除顯著降低了 DHOA 和 OA 的含量(圖 e,f),同時也減少了 α- 酮戊二酸,檸檬酸和乙酰輔酶 A 的含量(圖 g)。雖然天冬氨酸可以合成 DHOA 和 OA,外源添加天冬氨酸也并沒有使 DHOA 和 OA 的量增加(圖 e,f)。這些數據說明谷氨酰胺的 C 代謝和 N 代謝都與 DHOA 有關。
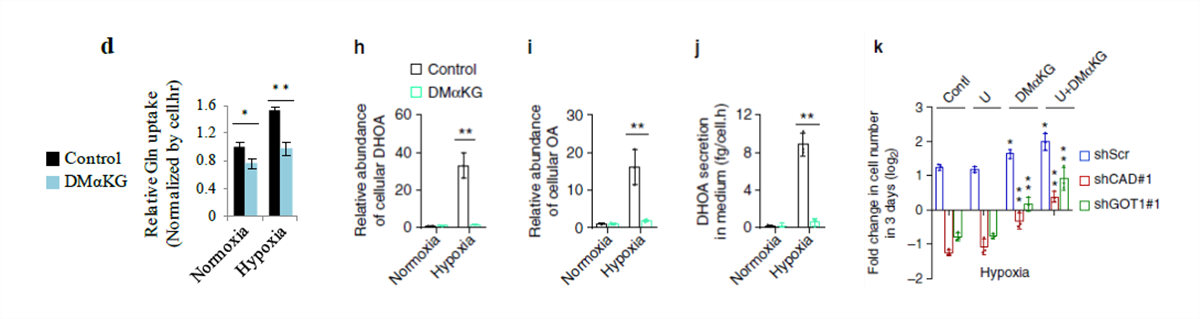
為了確認這個假設,使用 α- 酮戊二酸(C 來自谷氨酰胺)處理細胞,結果顯示 α- 酮戊二酸的添加可以減少谷氨酰胺的吸收(圖 d),幾乎完全清除了 DHOA 和 OA 的積累(圖 h,i),并且抑制了 DHOA 的分泌(圖 j)。尿苷和 α- 酮戊二酸的添加可以使敲除酶的細胞增值增加,但是單獨添加尿苷不能,單獨添加 α- 酮戊二酸或添加 α- 酮戊二酸和尿苷可以升高細胞的增殖,這些結果表明谷氨酰胺的 C 代謝對細胞生長來說是必要的,并且取決于 DHOA 的合成。
總結一下
通過同位素追蹤,文章展示了一條在缺氧條件下的谷氨酰胺通路,找到了缺氧條件下腫瘤細胞中的代謝變化,找到了谷氨酰胺的代謝產物 DHOA 和 OA, 并在病人和小鼠中也檢測到了升高的 DHOA 和 OA,因此他們可以作為腫瘤的潛在標志物,通路上的酶如 CAD 和 GOT1 可以作為腫瘤治療的可能目標。
怎么樣,代謝流的結果是不是很強大呢?
它可以為我們提供更直接的證據來說明問題,在基因工程和不同環境或不同代謝途徑中找到關鍵通路及代謝功能變化方面提供強有力的證據。